ΔTb m. Tb mol gula x 1000 berat air dalam gram.

Latihan Soal Kenaikan Titik Didih Larutan Sifat Koligatif Larutan Jempol Kimia
Kb air 0520Cm Ar Na 23 Ar O 16 Ar H 1 Pembahasan.

Contoh soal titik didih larutan. Kd molal air adalah 051. 27Contoh soal rumus kimia. Tb 08 T 0 b-Tb 08.
26Contoh Soal Kenaikan Titik Didih. 27Contoh soal sifat koligatif larutan kenaikan titik didih dan penurunan titik beku adalah sebagai berikut. Kenaikan titik didih larutan ialah selisih antara titik didihi larutan dengan titik didih.
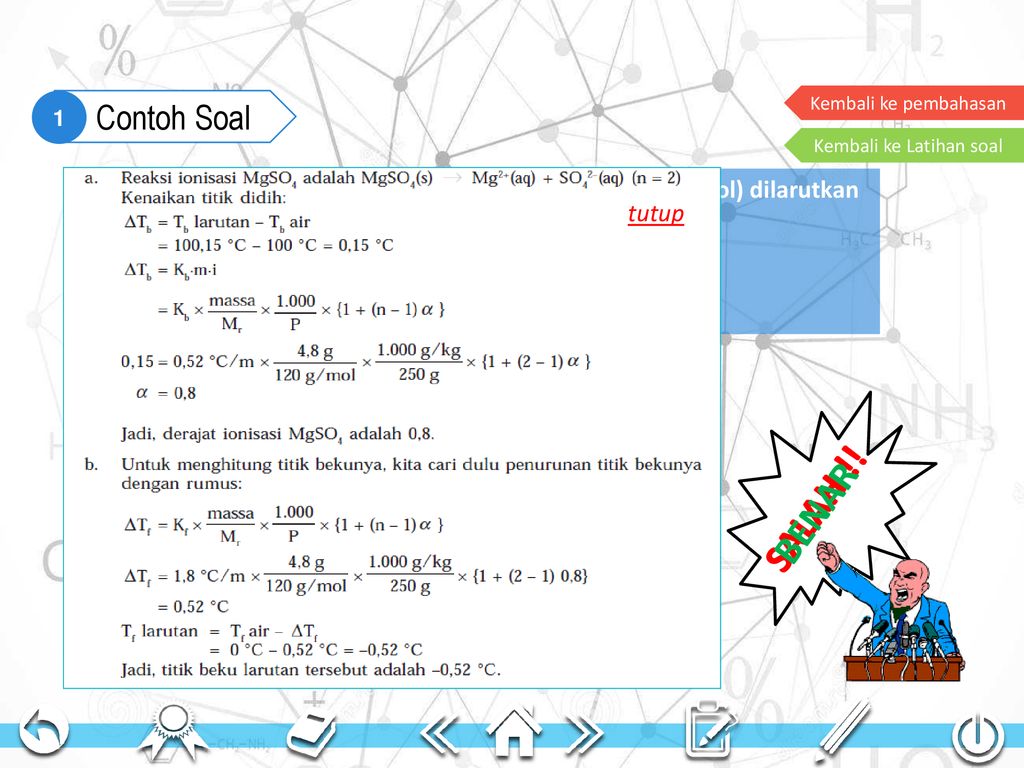
Untuk air murni T 0 b 100 o C. Larutan CaCl 2 dibuat dengan melarutkan 00169g dalam 1 Kg air suling dalam massa molar Ca 2 41g mol dan Cl 355gmol. Titik didih larutan ialah suhu pada ketika tekanan uap jenuh sebuah larutan sama dengan tekanan atmosfer di lingkungan kurang lebih.
Contoh soal penurunan titik beku kesimpulan jika 4 gram naoh dilarutkan dalam 100 gram air dan diketahui kb air 052 cm maka kenaikan titik didih larutan tersebut adalah 0104 c. Untuk kenaikan titik didih dan penurunan titik beku untuk larutan elektrolit perlu diperhitungkan faktor vant hoff sebagai berikut. Natrium hidroksida 16 gram dilarutkan dalam 500 gram air.
Tb 08 100 10080 0 C. Video ini dibuat untuk membantu siswai agar lebih memahami materi p. Tb 02 x 1000 250.
Berapakah berat molekul zat telarut. Maka pada tekanan uap jenuh larutan pada suhu berikut adalah. Jika Kf air 186 Cm tentukanlah titik beku larutan.
Jika pada tekanan osmotik pada 500 ml larutan fruktosa C6H12O6 dari suhu 32C sebesar 2 atm jumlah massa fruktosa yang dilarutkan adalah. Video ini membahas materi kimia Kelas XII MIPA yaitu Titik Didih Larutan Non Elektrolit. 4Kenaikan titik didih dapat ditulis sebagai.
Kenaikan titik didih larutan δtd. Jawaban contoh soal larutan. 7Bagaimana kedudukan titik didih larutan.
Hitung titik didih larutan tersebut. Koleksi Contoh Soal Kenaikan Titik Didih Dan Penurunan Titik Beku Larutan Terupdate. Contoh Soal Kenaikan Titik Didih.
Suatu larutan mengandung 324 gram zat yang tak mudah menguap juga nonelektolit dan 200 gram air mendidih pada 100130C pada 1 atmosfer. Kenaikan titik didih sebesar ΔT terjadi jika suatu zat yang masih murni solvent dicampur dengan zat lainnya sehingga berubah menjadi larutan solution yang memiliki titik didih yang baru dan lebih tinggi dari sebelumnya. 15Sebagai contoh titik didih normal air adalah 100 o C hal ini menyatakan bahwa tekanan uap air bernilai sama dengan tekanan luar yakni 1 atm.
Pada fraksi mol larutan urea didalam air 02. Tekanan uap jenuh air murni dengan suhu 20C sebanyak 175 mmHg. Tb 10013-100 013 Tb Kb x m 013 051 x m m 025 025 mol x 1000200 Mol 0255 005.
Hitung titik didih larutan tersebut. Kb grMr NaOH x 1000p x Kb. Gr 16 gr p 500 gr Kb 0520Cm Ditanyakan.

Sifat Koligatif Larutan Pengertian Rumus Dan Contoh Soal

Contoh Soal Kenaikan Titik Didih Dan Pembahasannya Soalfismat Com

Titik Didih Pengertian Kenaikan Rumus Dan Contoh Soal

Contoh Soal Kenaikan Titik Didih Larutan Sifat Koligatif Larutan Elektrolit Youtube
Contoh Soal Kenaikan Titik Didih

Contoh Soal Kenaikan Titik Didih Dan Pembahasannya Soalfismat Com

Soal Dan Pembahasan Sifat Koligatif Larutan Terlengkap Soalskul

Titik Didih Pengertian Kenaikan Rumus Dan Contoh Soal

10 Contoh Soal Sifat Koligatif Larutan Kenaikan Titik Didih Dan Penurunan Titik Beku Materi Kimia

Kenaikan Titik Didih Larutan Nonelektrolit
Rangkuman Kenaikan Titik Didih Dan Contoh Soalnya Tukang Ngetik

Sifat Koligatif Larutan Pengertian Rumus Contoh Soal

Contoh Soal Kenaikan Titik Didih

Contoh Soal Perbandingan Kenaikan Titik Didih Larutan Sifat Koligatif Larutan Elektrolit Youtube
Contoh Soal Dan Pembahasan Penurunan Tekanan Uap Dp Post 2 Chemistry Is Fun
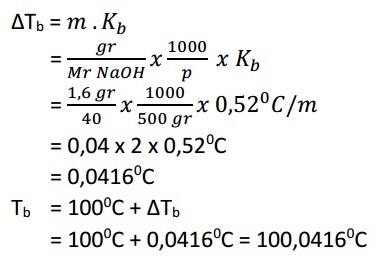
10 Contoh Soal Sifat Koligatif Larutan Kenaikan Titik Didih Dan Penurunan Titik Beku Materi Kimia

Terlengkap Rangkuman 100 Contoh Soal Sifat Koligatif Larutan

Contoh Soal Dan Jawaban Sifat Koligatif Larutan Elektrolit Penurunan Uap Jenuh Kenaikan Titik Brainly Co Id

All About Education Sifat Koligatif Larutan Kimia Xii
Source : pinterest.com